ワインを深く理解するために高校化学を振り返る第2回、有機化学について。
有機化学はレゴブロックと思ってください。
役割を持ったパーツを組み合わせて、無限のモノを形作ることができるのが有機化学です。
パーツの役割を知れば、その成分がどういう性質を持つのか予想できるようになります。
前後編ともに、奥田 大輔 さん @okkuudaaman に監修いただきました。
今回使用している化学構造式のイラストも奥田さんに作成頂いたものです。
お忙しい時間の合間を縫って、間違いの修正など無償でご協力頂いたことに感謝申し上げます。
有機化学とは
有機物とは炭素を多く含む物質の総称。私たちの身の回りにあるものどころか、私たち自身がほとんど有機化合物の集合体です。
有機化合物のややこしいところが2点。
無機化学なら例えばNaHCO3は炭酸水素ナトリウム(ベーキングパウダー)のように分子式で一つの物質に定まります。
しかし有機化合物は同じ分子式でも性質の異なる物質がたくさん存在するということ。この異性体の存在がややこしい。
また、多くの物質名が同じ特徴を持つ有機化合物の総称であることも理解を難しくします。
ワインを勉強していて目にする成分名に、高校で学習する範囲のものはほとんどありません。
しかしそのほとんどは、高校化学で習うパーツの組み合わせです。レゴで言うなら、基本的なパーツを使って小さなものはつくったことがあるけど、大きなものは未経験という状態なんです。
有機化学の基本を抑えた上で、ワインに含まれる成分までちょっとだけ背伸びしてみましょう。
有機化学は共有結合
無機化学編で紹介した通り、元素が結びついて分子をつくる際にいくつか方法があり、その一つが共有結合でした。
原子は最外殻電子が規定数まで埋まった状態が安定します。だから原子がくっついていくつかの電子を共有し、安定しようとするのです。
結合の手
例えばCH4メタンという非常にシンプルな物質があります。
炭素の最外殻電子は4。この軌道が安定する電子の数は8です。一方水素の電子は1で、電子2つの方が安定します。
なので4つの水素は炭素から一つずつ電子を借りる形で。炭素は水素と電子を共有して最外殻電子を満席にします。
こうしてメタンという物質は成り立っています。
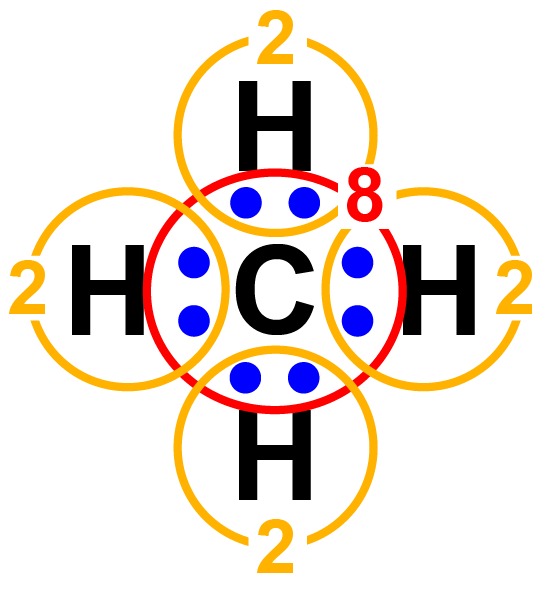
最外殻電子がいくつ足りないかを、「結合の手」という表現をします。
例えば炭素は最外殻電子4なので結合の手は4本。水素は最外殻電子が6であと2なので、結合の手は2本です。
結合の強さ
ひと口に共有結合といっても、結合の強さはいろいろです。
分解されにくい部分と、容易にほかの元素や分子に置き代わる部分があります。
結合の強さを決める要因のひとつは、共有電子の数です。
1個ずつの電子を共有しているものより、2個ずつの電子を共有しているものの方が結びつきが強い。
特に原子そのものが陽子1つである水素は、結びつきが弱くて他の元素や分子に置き代わりやすいです。
その置き代わるパーツは「炭化水素基」や「官能基」です。
官能基と炭化水素基
分解されにくい単位であり、何かしらの性質を示す゛パーツ"のことを「官能基」と呼びます。
これに関しては「こういうパーツがある」と覚えるしかありませんが、元素記号に比べると種類は少ないです。
代表的な官能基は次の通りです。
高校化学の代表的な官能基
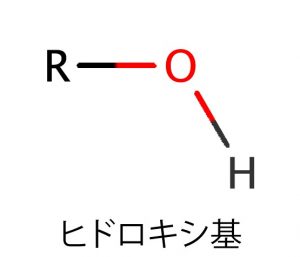
ヒドロキシ基 これがついていると水に溶けやすい
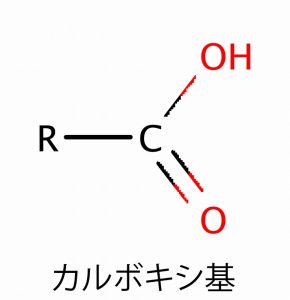
カルボキシ基 弱い酸性を示す
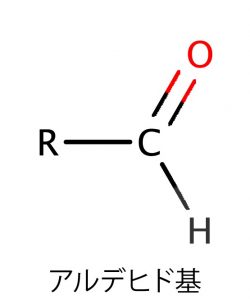
アルデヒド基 還元作用を示す
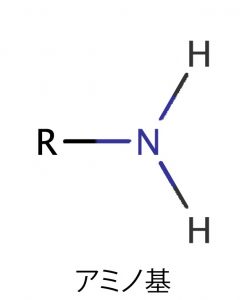
アミノ基 弱いアルカリ性を示す
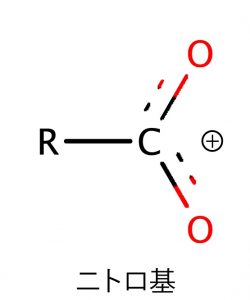
ニトロ基 酸化するとアミノ基になる。爆発性がある
Rのところにはいろいろな有機化合物が入ります。
これが、メタンCH4やエタンC2H6のように炭素と水素が連なった炭化水素基の水素原子と置き代わるようにくっついて、いろいろな有機化合物をつくります。
ベンゼン環
有機化学の基本的なパーツの一つに、分子式C6H6で表される「ベンゼン」という化合物があります。原油の成分のひとつです。
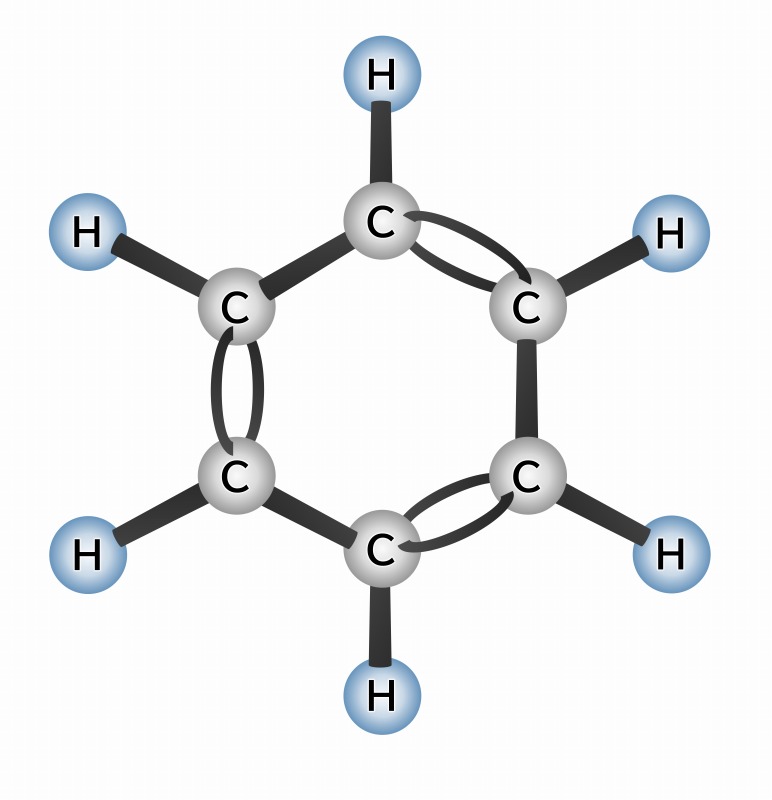
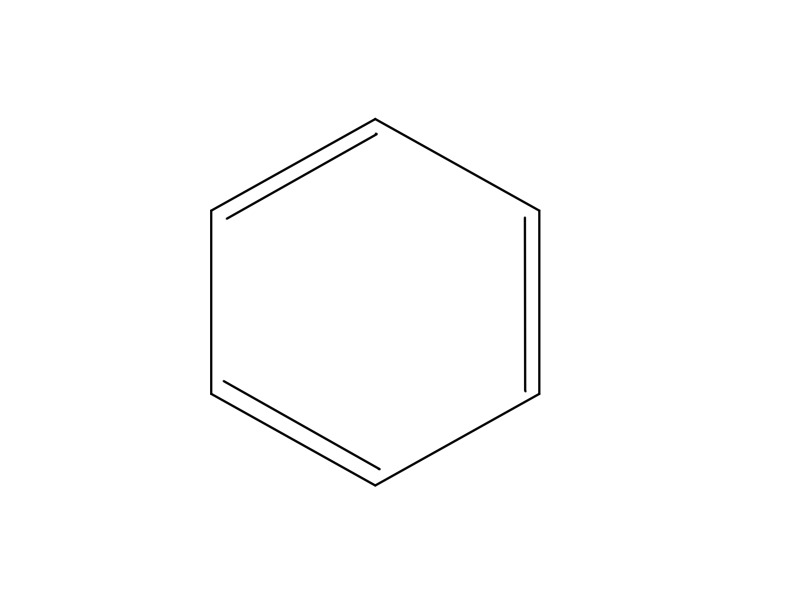
このような輪っか状に炭化水素がくっついた化合物を「芳香族炭化水素」と呼び、これまた非常に多くの仲間がいます。
その一つ。ベンゼンの水素をヒドロキシ基に置き換えたものが、皆様もよく目にする「フェノール」です。
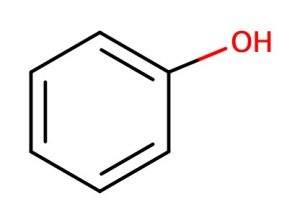
フェノール
実際にワインに含まれるのは、「フェノール類」や「ポリフェノール」と呼ばれるとおり、ベンゼン環にヒドロキシ基がついた様々な成分。「ポリフェノール」と呼ばれる化合物は5000種類以上確認されているといいます。
「フェノールとは亀の甲羅にOHがついたもの、ポリフェノールはそれがいっぱいくっついたもの」と覚えてください。
エタノールから酢酸へ
例えを紹介しましょう。ワインにとって最重要な有機化合物はエタノール、つまりアルコールです。
アルコールは分子式で表すならばC2H6O、これを性質が分かりやすいように文字で表す示性式に表すとC2H5OHです。
構造式で表すと次の通り。
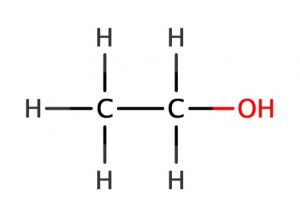
エチルアルコールの構造式
ちなみにアルコールとは炭化水素にヒドロキシ基がくっついた形の有機化合物の総称。
メチルアルコール(メタノール)やプロピルアルコール(プロパノール)などは、炭化水素基の部分の数が違うだけで性質は似ています。ただ、飲用に適するのがエタノールだけなので、アルコール=エタノールという認識なのです。
このエタノールに酸素が化合すると、
2CH3CH2OH + O2 → 2CH3CHO + 2H2O
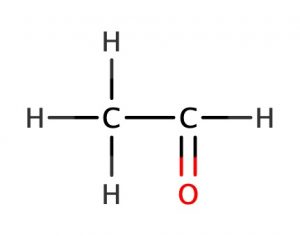
アセトアルデヒドの構造式
このように変化してアセトアルデヒドとなります。
アセトアルデヒドは二日酔いの原因と言われている物質です。
されにこのアセトアルデヒドもさらに酸素と結合し
2CH3CHO + O2 → 2CH3COOH
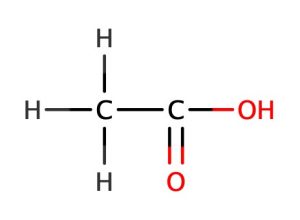
酢酸の構造式
つまり酢酸となって体から排出されます。
このように化学反応によって官能基が別の官能基に変化し、性質が変わることがあります。
異性体
分子式が同じでありながら結合の仕方が異なり、したがって性質も異なる物質のことを「異性体」と呼びます。
異性体にもどう違うのかで種類があり、「構造異性体」「幾何異性体」「光学異性体」があります。
構造異性体
先ほどのエタノールの例。C2H6Oという分子式は、このような構造式に並べることもできます。
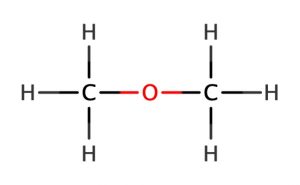
ジメチルエーテル
これも結合の手がきっちり埋まった安定した物質です。燃料として使われます。
こちらはヒドロキシ基はついていないため、アルコールとしての性質はありません。同じ分子式ながら全く別の物質なのです。
エタノールとジメチルエーテルの関係を、構造異性体といいます。
構造異性体は無限にある
例として挙げているのは、エタノールのような小さな分子であるため、構造異性体はそう多くありません。
しかし分子が巨大になると、いくらでも構造異性体が考えられるようになります。
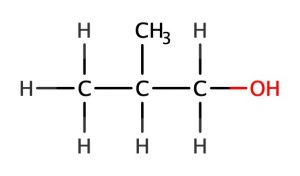
たとえばエタノールよりメチル基が2つ分多いブタノールC4H10O。
アルコールとしてのみで4つの構造異性体があり、それぞれ融点・沸点などの性質が違います。
しかし共通してアルコールとしての性質は持ちます。違うなりに共通点はあるのです。
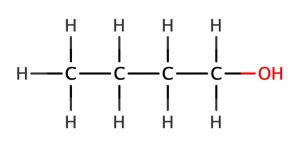 |
 |
|
 |
|
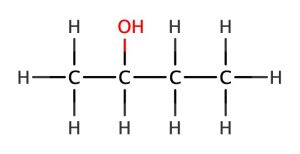
1-ブタノール
(n-ブチルアルコール) (一級アルコール)
融点:-90℃
沸点:117℃
|
2-ブタノール
(sec-ブチルアルコール) (二級アルコール)
融点:-114.7℃
沸点:99℃
|
2-メチルプロパン-1-オール
(イソブチルアルコール) (一級アルコール)
融点:-108℃
沸点:108℃
|
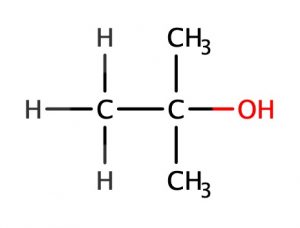
2-メチルプロパン-2-オール
(tert-ブチルアルコール) (三級アルコール)
融点:25.69℃
沸点:82.4℃
|
構造異性体だけでもややこしいですが、異性体はこれだけではありません。
幾何異性体と光学異性体
このパラグラフについては読み飛ばしてもらっても構いません。
知って頂きたいのは、「有機化合物は同じ名称でもいろいろなバリエーションがある。それは異性体の存在ゆえに」ということです。
「ピノ・ノワール」という名称とある程度共通するワインの特徴を持っていても、クローンの種類で樹の樹勢から収量から病気耐性からいろいろ違う。そんなものだと思って下さい。
幾何異性体があるのは二重結合を持つ有機化合物です。
例えば下記の構造式を持つ2-ブテンという化合物。炭素の結合の手を2重につないでいるところがあります。
結合の手は1本だと捻ることができますが、2本だと平面上に向きが固定されます。この2重結合を中心に、炭素結合が同じ側にくっつくか、反対側にくっつくか。これがシス - トランス異性体です。
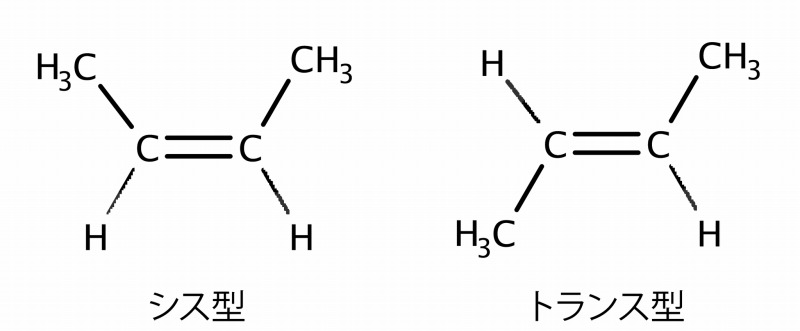
よく「トランス脂肪酸ゼロのマーガリン」などという謳い文句があるでしょう。これはトランス型の結合をしている脂肪酸という意味です。(脂肪酸については後述)
炭素の4つの結合の手がつなぐもの。それが4つとも違うパーツだった場合は「光学異性体」を持ちます。
正三角錐の中心に炭素があり、それぞれの頂点に違うパーツがついているとします。R1,R2,R3、R4としましょう。
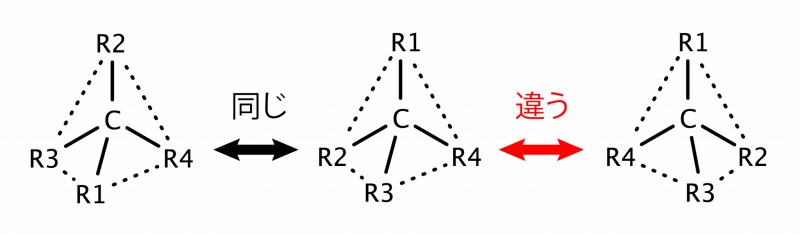
真ん中の構造を回転させることで、左とは同じにできますが、右の構造にすることはできません。
パーツのついている向きが違うだけ。これを光学異性体といいます。
光学異性体が異なれば、生理活性が違うといいます。つまり味が違うという場合もあるのです。
光学異性体の関係は互いに変化することもあるので、ワインの味わいの変化には光学異性体の変化も関係しているかもしれません。(かなり分析が難しいので、実証はできないと思います)
有機化合物はなかなか特定できない
無機化合物みたいに、「〇〇という物質は分子式が△△でこのような構造をしている」といえるなら簡単。ワインで知らない化合物が出てきたときも、WilipediaかGoogle先生が分かりやすく教えてくれます。
しかし有機化合物においては、「■■基を持つものの総称」のように、どうにもよくわからない答えがほとんど。
これは有機化合物はパーツの組み合わせで無限といえるほどの種類の化合物が考えられるから。
さらに性質が少し異なる「異性体」があるからです。
しかし「官能基」とよばれる性質を持ったパーツの特徴や、その化合物の大きさなどから、なんとなく性質が想像できます。
ここからはワインでよく目にする成分を、これまでに紹介した知識をもとに見ていきましょう。
ワインに関係する有機化合物
ワインの成分としてよく目にする化合物のうち、高校の教科書に載っているものは、実はあまり多くありません。
ただ、高校で習うことをきっちり理解できていれば、ちょっと背伸びするだけで分かりそうなものもたくさんあります。
ワインに役立つ有機化学をちょっとだけ紹介します。
香り成分に関係する「揮発」とは
ワインに含まれる成分のうち、香りに関係する成分は比較的わかりやすい。
というのも香りに感じるということは揮発するということで、比較的分子のサイズが小さいからです。
揮発とは蒸発しやすいことです。液体から気体になる沸点が低いものは、揮発しやすい傾向にあります。
例えば、皮膚が水に濡れるのとアルコールに濡れるのだと、アルコールの方が冷たく感じます。
これはアルコールの方が水よりも沸点が低く揮発しやすいため、気化熱を奪って蒸発するから冷たく感じるのです。

揮発しやすいかどうかは、化合物の分子量だけでなくいろいろな要因が影響しますが、軽いものほど揮発しやすい傾向にはあります。
ただし揮発しやすいから香りとして強く感じるとは言えません。香りを感じる濃度「閾値」というものがあって、非常に小さな濃度でも感じる香りもあれば、かなりの量漂わないと気づかない香りもあるのです。もちろん個人差もあります。
揮発酸とは
時々ワインのネガティブな香りとして名前が挙がる「揮発酸」。蒸発しやすい性質を持つ酸という意味で、ワインの中には酢酸、葉酸、プロピオン酸、ブチル酸などが含まれているといいます。
ここで問題になるのが酢酸と、酢酸がアルコールと反応してできる「酢酸エチル」です。
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
酢酸エチルは常温では液体で、沸点77度と低く蒸発しやすい性質を持ちます。いろいろな成分を溶かすことができる有機溶媒として広く使われており、セメダインにも入っていますし、マニキュアの除光液などにも使われます。
個人的には「トラバルーン」という子供のころ遊んだ風船のおもちゃの臭いと認識しています。この溶媒も酢酸エチルです。
全てのワインに含まれていますが、少量ならパイナップルのようなフルーツの香りに感じ、問題になることはありません。日本酒の香り成分でもあります。
しかし酢酸エチルの香りがあまりに強いと、ワインがその香りに支配されてしまうため、欠陥香とみなされます。
ワインの酸味成分 酒石酸
続いてワインに重要な酸味成分を見てみましょう。酒石酸、リンゴ酸、クエン酸が特に重要な酸味成分です。
まずは酒石酸。一番多く含まれる酸味成分です。次のような構造式を持ちます。
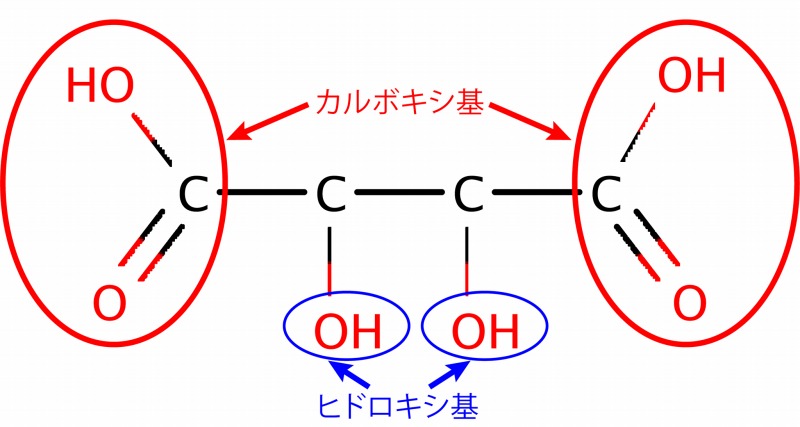
2つのカルボキシ基を持っているので、水に溶けると水素イオンを放出し酸性を示します。
放出した水素イオンの代わりに、金属イオンがくっついて塩となることがあります。ワインの場合はカリウムかカルシウムと結合することが多いです。
酸味の高い、つまり酒石酸濃度の高いリースリングなどのワインが熟成すると、白や透明の結晶が沈殿することがあります。
この色の違いはどうやらカリウムかカルシウムの違いのようで、無色の結晶をつくるのが酒石酸カルシウムです。
ワインの酸味成分 リンゴ酸と乳酸
続いてリンゴ酸ですが、酒石酸と非常に似た構造式を持ちます。ヒドロキシ基の一つが水素に置き代わったものです。
(有機化学の構造式において、しばしば炭素につく水素は省略されます)
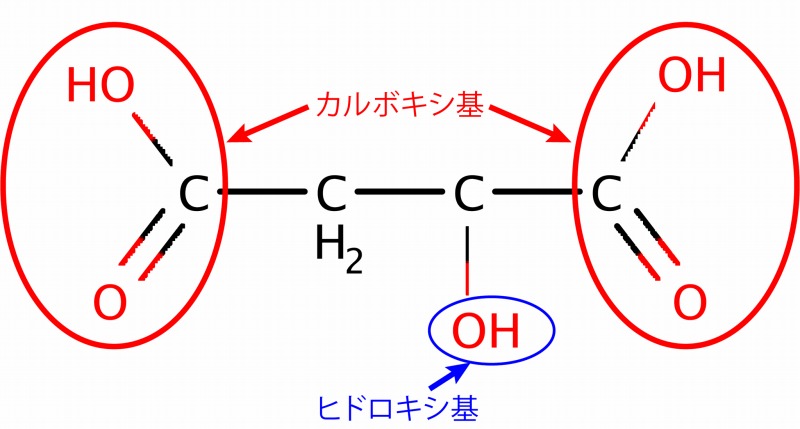
リンゴ酸と聞いたら、ソムリエやワインエキスパートを受けた方なら「マロラクティック発酵」を思い浮かべるでしょう。
リンゴ酸(malic acid)を乳酸(lactic acid)に変える反応を言います。正確には乳酸と二酸化炭素に分解されます。
乳酸の化学式は次のとおり。
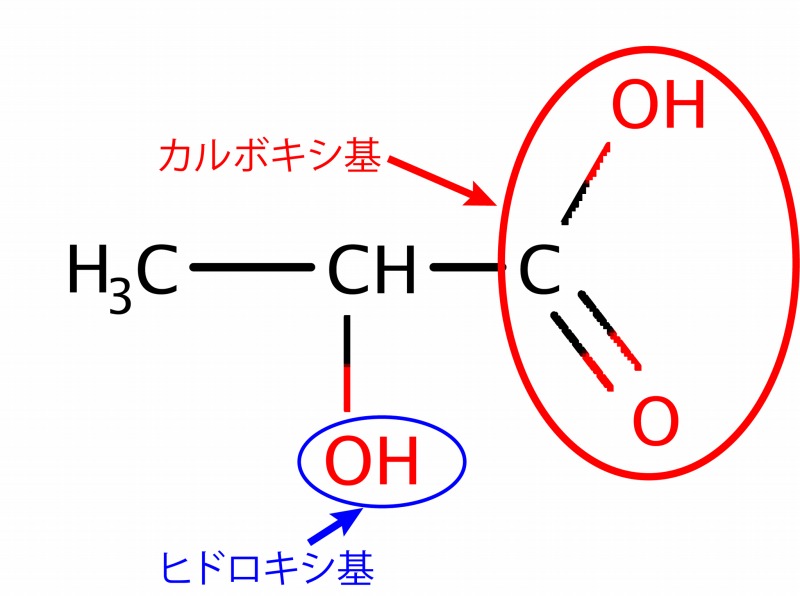
ヒドロキシ基がない方のカルボキシ基がなくなってしまいました。
2価のリンゴ酸と異なり、乳酸は1価の酸なので酸が弱くなる、酸味が穏やかになるのです。
ワインの酸味成分 クエン酸
クエン酸はさらにカルボキシ基が多く、3価の酸です。
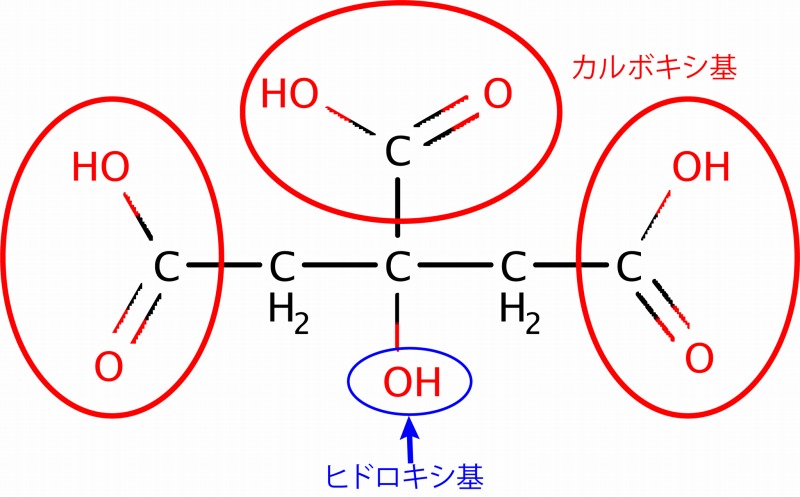
レモンなどの柑橘系フルーツに多く含まれている酸味成分です。
前半の無機化学編で中和滴定のお話をしました。
中和滴定の結果は酸味成分が全て酒石酸であったと仮定して算出されます。これを「酸度」といいます。
一般的には1Lのワイン中に含まれる酒石酸のグラム数として、「g/L」の単位で表記されます。
(日本では国税庁所定の分析法に従い、100mL中の酒石酸の質量(g/100mL)で表記されます。意味するところは全く同じですが、値は10倍違います。)
TCA トリクロロアニソール
ワイン好きの天敵といえる有機化合物が、「TCA」の略称である2,4,6-トリクロロアニソールでしょう。
コルクの欠陥でワインをダメにしていまう「ブショネ」の原因物質です。
この「2,4,6-」というのは、官能基がつく場所を示す数字です。
「トリ」というのが「3つの」という意味で、「クロロ」つまり塩素(Cl)が3つ結合していることを示します。
この命名法についてはあまり気にしなくていいでしょう。
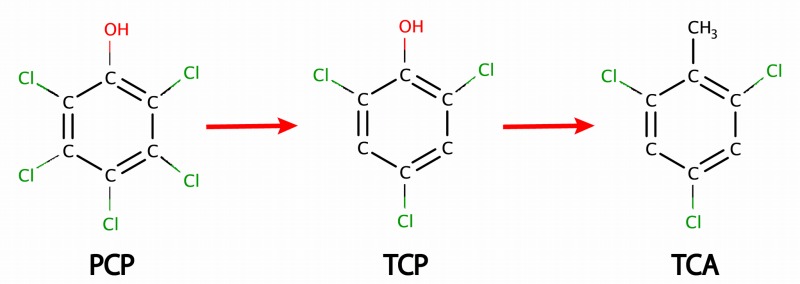
まずペンタクロロフェノール(PCP)と呼ばれる、木材を殺菌・保存するための薬剤があります。
それが光やカビなどの影響で、2,4,6-トリクロロフェノール(TCP)という物質に変化します。
土壌に含まれるストレプトマイセス属という細菌がこのTCPを代謝することで、2,4,6-トリクロロアニソール(TCA)を作り出してしまうのです。
アミノ酸とは
ワインに限らず日常的に目にする「アミノ酸」。
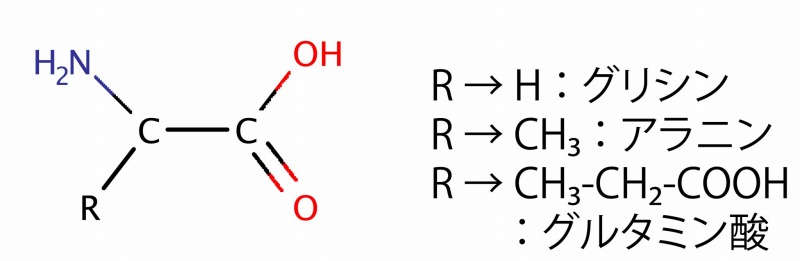
化学的には、カルボキシ基とアミノ基の両方を持つ有機化合物の総称です。
自然界には約500種類確認されており、そのうち20種類は私たちの体の構成要素です。
Rのところに入るパーツによって、アミノ酸の種類が決まります。
タンパク質
アミノ酸はアミノ基とカルボキシ基が結合することで、大きな分子を作ります。そんなに大きくないアミノ酸の塊を「ペプチド」。巨大なものを「タンパク質」と呼びます。タンパク質が人体にとって重要であることは言うまでもないでしょう。
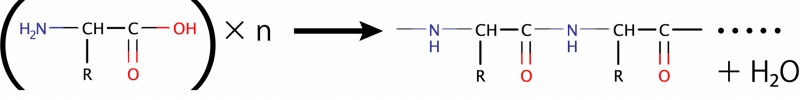
nには適当な数字が、Rにはアミノ酸の種類に応じてパーツが入ります。
いくらでも、とは申しませんがタンパク質は非常に多くのアミノ酸の集合体です。
分子量4000程度なら小さいほう。(全部グルタミン酸だとして27個くらい)
巨大なものだと分子量数千万から億単位になると言います。
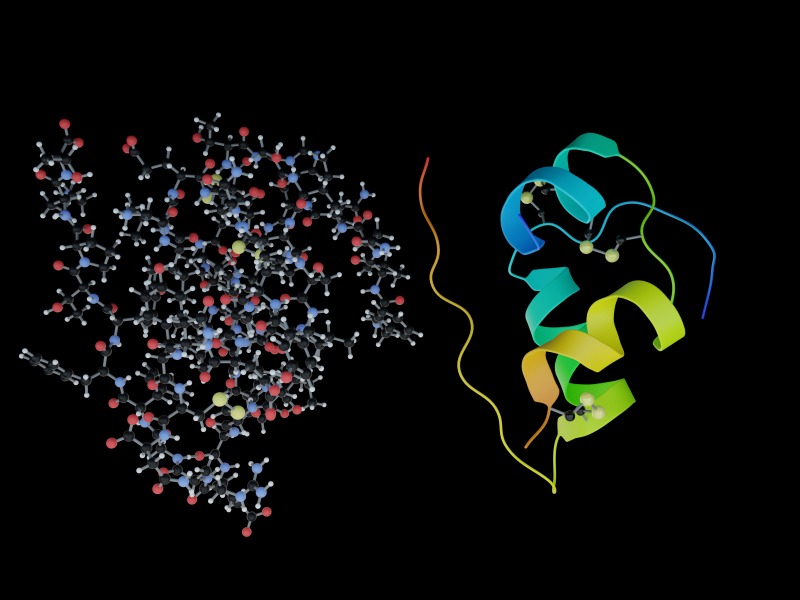
人体は20種類のアミノ酸が複雑に結合しタンパク質をつくることで構成されています。
20種類のうちいくつかは食物から合成する能力を持ちますが、9種類のアミノ酸は体内で合成できず、食べ物から摂取する必要があります。
それもあって、アミノ酸は「美味しく」感じるのでしょう。
例えばグルタミン酸。昆布やチーズ、椎茸やトマトに多く含まれるうま味成分です。「味の素」などの化学調味料の主材料の一つでもあります。(グルタミン酸は必須アミノ酸というわけではありません。)
タンパク質の分解
タンパク質とアミノ酸と聞いてワイン好きが思い浮かべるのは、スパークリングワインの瓶内2次発酵による酵母の自己分解ではないでしょうか。
酵母とは「単細胞性の菌類」の総称と定義されています。
この分類的なものは私に生物の知識が乏しいのでよくわかりません。ともあれ、タンパク質などで構成されているのは間違いない。タンパク質はそのサイズが大きいものが多いため、水やワインに溶けず沈殿していることが多いです。
瓶内2次発酵が終わると酵母は死滅し、タンパク質は分解されていきます。その分解とは、上記のアミノ酸がつながる反応の逆。水がくっつくことで結合の鎖が切られるのです。「加水分解」といいます。
そうして小さな塊となったアミノ酸やペプチドは溶けやすく、ワインの中に戻っていきます。こうして熟成シャンパンなどに感じる「うま味」となるのです。
このたんぱく質の分解、体内では分解を助ける「酵素」というものがあるのですぐに消化されますが、ワイン中では非常に時間がかかります。非常にゆっくりと進む反応です。
「瓶内2次発酵したスパークリングワインの特徴は、パンだねやブリオッシュなどの香り」なんて言われます。しかしシャンパンの規定である15か月程度では、私は感じたことがありません。経験的に3年を超えたくらいからものによって感じ、5年を超えるくらいから多く感じます。
重合反応
重合反応とは、ある分子が何かしらの結合方法で、単位分子の繰り返しとして何百・何千とくっつくことを言います。
プラスチックと呼ばれるような高分子有機化合物は、このようにつくられます。
付加重合
炭素の2重結合を持つ基本的な単位分子が、その二重結合を開いてたくさんくっつくことを付加重合といいます。
例えばエチレンC2H4。炭素は4つの結合の手があるところ、2つは水素で埋まり、もう2本は炭素と2重につないでいます。
このつないだ手を別の炭素に繋ぎ変えることで、エチレンがたくさん結合できるようになります。これがポリエチレン。
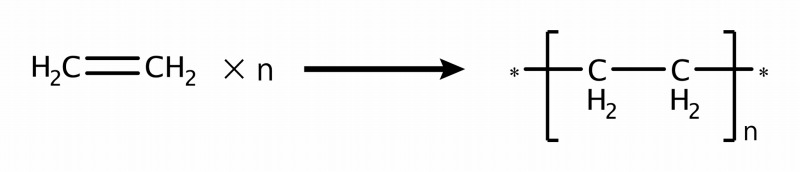
使い捨ての手袋などに使われる素材です。

こうして基本的なパーツがたくさん集まってできる高分子化合物を「ポリマー」と呼びます。
この付加重合を起こす CH2=CH- を「ビニル基」と呼び、この重合でできる高分子化合物の総称が本来の意味の「ビニール」です。
ビニル基にベンゼン環がついたもの、エチレンの水素のひとつがベンゼン環に変わったものが「スチレン」。
これが付加重合をすると「発泡スチレン」となります。
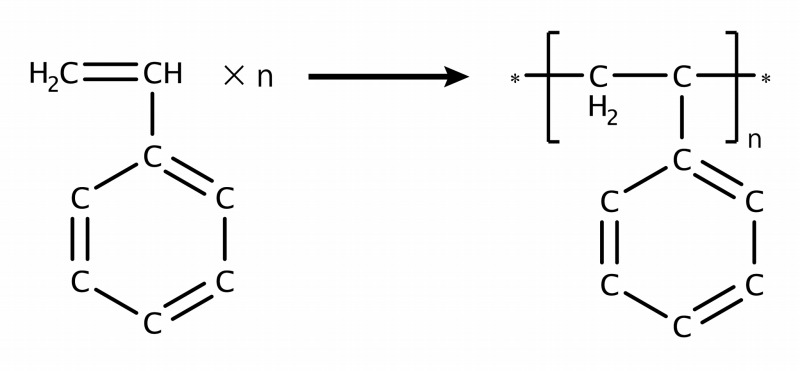
スーパーでお肉などの販売に使われているトレーは、この発泡スチレン製です。
飽和脂肪酸と不飽和脂肪酸
このビニル基のような炭素の二重結合を持つものを「不飽和~~」といいます。
脂肪酸とは炭化水素がいくつも連なったものにカルボキシ基がついているものを言います。
一番単純な脂肪酸が酢酸、CH3-COOHです。
そして飽和・不飽和というのは、炭素の結合の手が余っているかいないかの違いです。
炭素の結合の手は、余っていれば2重結合をつくり、余っていなければ水素と結合しています。
CH3-CH2-CH2-・・・・CH2-COOHというのが飽和脂肪酸。
肉や牛乳、バターなどに多く含まれ、取りすぎは心血管疾患のリスク増大につながると言われています。
それに対して、いわゆる「体にいい油」のように言われているのは、不飽和脂肪酸です。中でも幾何異性体としてトランス結合のないもの、シス結合のみのものが体にいいのでしょう。
(この記事の体にいい・悪いについては全く保証しません。話半分に読んでください)
たとえばリノレン酸。アマニ油やエゴマ油に多く含まれているといいます。構造式はこのようなもの。
※分子量が大きくなる有機化学では、基本となるCとHは省略されます。折れ線部にはCH、CH2、CH3が省略されていると考えてください。
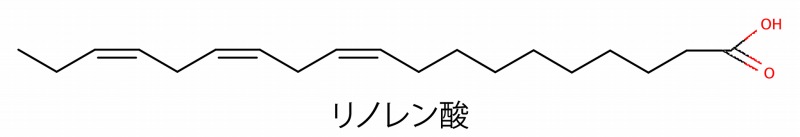
このリノレン酸やエイコサペンタエン酸、ドコサヘキサエン酸は、人体では合成できず食物から摂らないといけない必須脂肪酸です。
縮合重合
先ほどのアミノ酸の結合のように、くっつくことで水分子が取れるものの重合を「縮合重合」といいます。
高校化学で習うその代表格が、ポリエチレンテレフタラート、つまりPETボトルです。
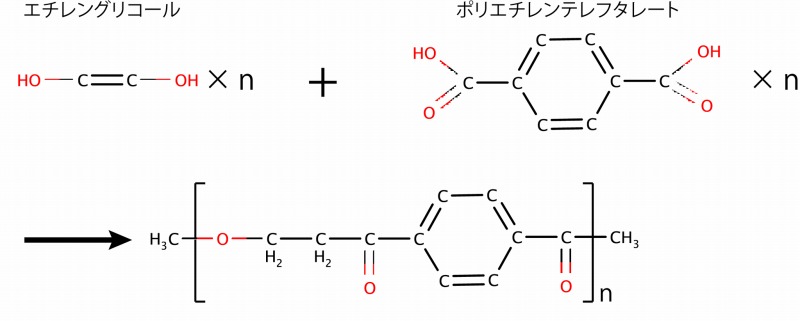
エチレングリコールもテレフタル酸も今回初めて出てきた物質です。
でも起こっている反応といえば、ヒドロキシ基とカルボキシ基がくっついているだけ。先に説明した酢酸とエタノールから酢酸エチルができるのと本質的には同じです。

多くの自治体で、卵パックや食品トレーなどの燃えないゴミとペットボトルの回収は別でしょう。
「仕分けがめんどくさいな~」と思っているのは私だけではないはず。
しかしその構造にこれほど違いがあると知れば、そりゃあ一緒にしたら再生に困るのがわかるはず。地球のためにがんばって分別しましょう。
バッグインボックスは酸化していく
紙の箱に入った3Lくらいのワインを見たことがあるでしょうか。
たいていは手ごろなワインに使われます。段ボールの箱の中にプラスチック系の袋に入ったワインが収められており、注ぎ口がついています。
「空気が入らず劣化しにくいので1か月くらい楽しめる」というのが謳い文句です。
通常のガラス瓶ワインと比べて、飲みたいだけ飲めます。容量の割に容器が軽く、輸送コストも安くてエコです。ゴミも出しやすい。
ただし、長期保存は全くできません。それはプラスチック系の袋だから。性質上、微量の酸素を通してしまうからです。
(数カ月単位なら問題ないでしょう)
プラスチック系素材の袋は、上記の重合反応でできた有機化合物でつくられます。これは糸を編み込んで布をつくるようなもの。だからどうしても空気の分子程度の大きさなら通してしまうのです。
これはゴムでも一緒。タイヤの空気が時間と共に抜けていくのは、そういう性質なのです。

だから本当に空気を遮断したければ、素材は金属でないといけません。
前編で述べたように、金属は原子核が並んだ周りを自由電子が飛び回っています。その自由電子が空気の透過を遮断します。
そういう意味では、アルミ素材でパウチされたものは、より保存がききます。
バッグインボックスはガラス瓶にコルク栓のワインと比べて、はるかに早く劣化します。袋の素材が微量の酸素を通すからです。
有機素材の性質を知っていれば、年単位で売れ残っていそうなバッグインボックスのワインには手を出す気になれません。
ワインを深く知る助けに
ワインを楽しく飲むうえで、化学の知識は必須ではありません。きっと仕事で役にたつという方もそう多くはないでしょう。
しかし、必要ではないからこそ知って楽しむのが趣味であり娯楽なんです。そもそもワインは好きで飲んでいますよね。
「この2本のワイン、大きく風味が違うけど、それはなぜだろう?」
その疑問に対して、化学は時に“それらしい”理由を示してくれます。それが納得できた時の気持ちよさ。「そんなの必要ない」とは言い切れないでしょう。
(ワインの味という結果には様々な原因が絡み合うので、簡単に言い切ることはできません)

「このワインの香り、モノに例えるとしたら何だろう?」
それが言葉にできたとき、そのワインはあなたの記憶により深く刻まれるはず。言葉は認識を助けます。
例えば酢酸エチルなどは、それが含まれる他のモノの名前を示されることで、次からきっと認識しやすくなるはず。
正直、高校化学の知識で説明できない化合物は、ワインの中にはたくさんあります。私もあまり分かってないところがほとんどです。
それでもこの記事を通して、知らない化合物の名前に対する苦手意識が少しでも少なくなれば幸いです。
【あとがき】
こうやって文字に起こすことで、自分の理解が弱いところが明らかになる。わからないところが見つかるものです。
ところで、ソムリエってなんでしたっけ?